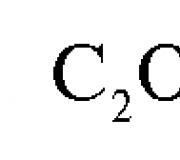Соль представляет собой бесцветные ромбические кристаллы. E515 Сульфаты калия
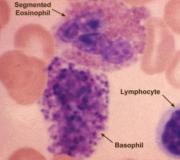
Принцип методаПри проведении пероксидазной реакции цитоплазма лейкоцита приобретает голубую или синюю окраску.
Необходимые реактивы
Краситель - 300 мг диаминофлуорена и 130 мг флюксина В растворяют в 70 мл 95%-ного этанола. К этой смеси добавляют 11 г ацетата натрия (CH3COONa ґ 3Н2О), растворенного в 20 мл 0,5%-ной уксусной кислоты, и 1 мл 3%-ной перекиси водорода. Через 48 ч реактив фильтруют, и он становится годным к употреблению. Хранить его необходимо в темной, химически чистой посуде и периодически фильтровать.
Ход исследования
10 мл свежевыделенной мочи фильтруют через фильтровальную бумагу, после чего на бумагу наносят 3 капли красителя. При содержании в 1 мкл мочи более 10 лейкоцитов на месте нанесения краски появляется темно-синее пятно. Проба считается отрицательной, если пятно красного цвета, и сомнительной, если пятно голубого цвета.
Проба проста и достаточно надежна, ответ можно получить через несколько минут.
Экспресс-метод выявления скрытой лейкоцитурии имеет большое значение при профилактических осмотрах, особенно детей в яслях, детских садах и школах.
При положительном значении этой пробы лейкоцитурия выявляется и всеми другими методами, используемыми для ее количественного определения.
Неорганизованный осадок мочи
Неорганизованный осадок мочи состоит из солей, выпавших в осадок в виде кристаллов или аморфных масс. Характер солей зависит от коллоидного состояния мочи, рН и других свойств. При кислой реакции мочи обнаруживаются:
1) мочевая кислота - полиморфные кристаллы (ромбической, шестигранной формы, вид бочонков, брусков и др.), окрашенные в желтый цвет (иногда бесцветные). Кристаллы мочевой кислоты растворяются в щелочах, не растворяются в кислотах. Макроскопически в осадке мочи имеют вид золотистого песка;
2) ураты - аморфные мочекислые соли. Располагаются кучками желтовато-коричневатого цвета. Растворяются при нагревании и при добавлении щелочей.
При действии кислот (уксусная или соляная) постепенно превращаются в бесцветные кристаллы мочевой кислоты ромбической формы. Макроскопически ураты после центрифугирования имеют вид плотного кирпично-розового осадка. В таких случаях необходимо освободиться от солей, так как они мешают микроскопическому исследованию. С этой целью используют реактив Селена (4 г буры и 4 г борной кислоты растворяют в 100 мл дистиллированной воды). В центрифужную пробирку после удаления надосадочной мочи наливают реактив Селена, смешивают, центрифугируют вновь и микроскопируют осадок;
3) щавелевокислая известь (оксалаты) встречается в кислой моче, но может быть и в моче со щелочной реакцией. Кристаллы имеют форму октаэдров (“почтовые конверты”), а также круглую или овальную форму. Растворяются в соляной кислоте, не растворяются в щелочи и уксусной кислоте;
4) углекислый кальций обнаруживается в форме мелких шариков. Растворяется в кислотах, выделяя углекислоту.
При щелочной реакции мочи обнаруживают:
1) кислый мочекислый аммоний (в моче детей может быть при кислой реакции).
Имеет форму гирь и шаров, часто с отростками. Растворяется при нагревании и в щелочах. При добавлении кислот (соляной или уксусной) образуются бесцветные ромбические кристаллы мочевой кислоты;
2) трипельфосфаты - бесцветные кристаллы в форме “гробовых крышек”. Растворяются в кислотах, не растворяются в щелочах;
3) фосфаты - аморфные массы солей сероватого цвета часто вместе с трипельфосфатами. Растворяются в кислотах, не растворяются в щелочах. Макроскопически осадок белого цвета;
4) нейтральная фосфорнокислая известь - кристаллы клиновидной формы, часто располагающиеся розетками, бесцветные (иногда могут быть в моче при слабокислой реакции). Растворяются в кислотах, не растворяются в щелочах.
Особого диагностического значения неорганизованный осадок не имеет. Большое количество кристаллов мочевой кислоты и уратов встречается при лихорадочных состояниях, процессах, связанных с массивным распадом клеток (лейкозы, опухоли), при почечно-каменной болезни и др.
В патологической моче встречаются:
1) цистин.
Имеет вид шестигранных бесцветных прозрачных плиток, обнаруживается при кислой реакции мочи. Растворяется в щелочах, аммиаке, минеральных кислотах. Не растворяется в уксусной кислоте, спирте, ацетоне, эфире;
2) тирозин - кристаллы в виде тонких игл, собранных в пучки. Обнаруживается в моче с кислой реакцией. Растворяется в щелочи, минеральных кислотах. Нерастворим в спирте, ацетоне, эфире;
3) лейцин - блестящие мелкие шары с радиальной и концентрической исчерченностью. Встречаются в моче с кислой реакцией. Растворяются в минеральных кислотах и щелочах. Нерастворимы в спирте, ацетоне, эфире.
Нахождение этих кристаллов имеет диагностическое значение, поэтому для распознавания их недостаточно одних морфологических признаков. Необходимо использовать все микрохимические реакции, характерные для них, так как некоторые формы этих кристаллов имеют сходство с кристаллами мочевой кислоты, жиром, нейтральной фосфорнокислой известью.
Кристаллы лейцина, тирозина и цистина обнаруживаются при подострой дистрофии печени, отравлениях фосфором;
4) жирные кислоты имеют вид тонких игл, иногда собранных в пучки. Встречаются редко, при патологических процессах, сопровождающихся жировой дистрофией и распадом клеток;
5) холестерин имеет вид тонких четырехугольных бесцветных пластинок с обломанным углом. Обнаруживаются при патологических процессах, сопровождающихся распадом и жировой дистрофией клеток. В моче встречается редко;
6) билирубин - кристаллы в виде мелких желтовато-коричневых иголок, складывающихся в пучки или в виде зернышек. Обнаруживаются в моче с желчными пигментами. Билирубин растворяется в щелочах и хлороформе. С азотной кислотой дает зеленое окрашивание;
7) гематоидин - кристаллы в форме ромбов или иголок, которые могут складываться в пучки и звезды. Цвет золотисто-желтый. Являются продуктом распада гемоглобина. В своей молекуле не содержат железа. Образуются в некротизированной ткани, в глубине гематом и в больших участках кровоизлияний;
8) гемосидерин - золотисто-желтые аморфные зернышки, находящиеся внутри клеток (в отличие от гематоидина). Представляет продукт распада гемоглобина и дает положительную реакцию на берлинскую лазурь, так как содержит железо. Обнаруживается при внутрисосудистом гемолизе (болезнь Маркиафава-Микели);
9) липоиды обнаруживаются в поляризационном микроскопе, где они дают двоякое преломление света. Двоякопреломляющие свет капли жира внутри- и внеклеточные имеют вид блестящего креста на темном фоне. Обнаруживаются при нефрозах (особенно амилоидно-липоидных);
10) лекарственные кристаллы встречаются при приеме некоторых медикаментов. Кристаллы пирамидона выпадают в виде коричневатых иголок, похожих на кристаллы билирубина, но длиннее, образующих пучки и звезды. Цвет мочи при этом розовато-красноватый. Кристаллы сульфаниламидных препаратов отличаются большим полиморфизмом. Почти всегда окрашены в желтоватый цвет, имеют вид снопов, шаров, брусков и т.д. Многие из них имеют сходство с кристаллами мочевой кислоты. Распознавание их производится при помощи индикаторной бумажки.
Приготовление индикаторной бумаги
Фильтровальную бумагу пропитывают реактивом (см. ниже), высушивают, нарезают тонкими небольшими полосками, хранят в темном месте. Полоску бумаги опускают в осадок мочи. В присутствии кристаллов сульфаниламидных препаратов бумажка дает моментальное ярко-желтое окрашивание.
Реактив: 1 г пара-диметиламидобензальдегида, 2 мл концентрированной НСl, 98 мл 2,24%-ного раствора химически чистой щавелевой кислоты.
Натрия сульфат (Сернокислый натрий) – натриевая соль серной кислоты.
Физико-химические свойства.
Химическая формула Na 2 SO 4 - натрия сульфат (натрия сульфат безводный, натрий сернокислый безводный, тенардит). Бесцветные ромбические кристаллы. Плотность 2,7 г/см 3 . Температура плавления 884°С. Безводный сульфат натрия устойчив выше температуры 32,384 °C, ниже этой температуры в присутствии воды образуется кристаллогидрат Na 2 SO 4 ·10H 2 O (десятиводный сернокислый натрий).
Формула Na 2 SO 4 ×10H 2 O - десятиводный сернокислый натрий (натрия сульфат декагидрат, глауберовая соль, мирабилит). Большие бесцветные призматические кристаллы моноклинной системы, горько-соленого вкуса. Плотность 1,46 г/см 3 . Температура плавления 32,384 °C. Температура разложения 32,384 °C. На воздухе разлагается на безводный натрия сульфат и воду. Нормально растворим в этаноле. Хорошо растворим в воде.
Применение.
Применяется сульфат натрия как один из основных компонентов шихты в производстве стекла; при переработке древесины (сульфитная варка целлюлозы), при крашении хлопчатобумажных тканей, для получения вискозного шелка, различных химических соединений - силиката и сульфида натрия, сульфата аммония, соды, серной кислоты. Натрий сернокислый применяется в строительстве как противоморозная добавка и ускоритель схватывания бетонной смеси. Также сульфат натрия применяется в производстве синтетических моющих средств; растворы сульфата натрия используются в качестве аккумулятора тепла в устройствах, сохраняющих солнечную энергию.
Применение сульфата натрия в производстве стекла.

Сульфат натрия применяют преимущественно как осветляющую добавку в количестве от 3 до 10%, в зависимости от количества соды. Он вводится в состав сырья не только как источник Na 2 O , но и SO 3 , который необходим для повышения скорости осветления стекломассы. Ранее соотношение сульфата натрия и соды составляло 1:6, в настоящее время – 1:20. Это диктуется необходимостью уменьшения количества SO 2 в дымовых газах. Сульфат натрия в шихте листового и бесцветного тарного стекла характеризуется специфическими реакциями.
Например, в содовой шихте натрий-кальций силикатного стекла происходят следующие процессы:
…………………………………………………………………………………………………Температура, °С
Образование CaNa 2 (CO 3) 2 ……………………………………..……….ниже 600
CaNa 2 (CO 3) 2 + 2SiO 2 > CaSiO 3 + Na 2 SiO 3 + 2CO 2 ………………….. 600-830
Na 2 CO 3 + SiO 2 = Na 2 SiO 3 + CO 2 ………………………………………...720-830
Образование плавней и эвтектики
CaNa 2 (CO 3) 2 - Na 2 CO 3 …………………………………………………..740-800
Плавление двойного карбоната CaNa 2 (CO 3) 2 …………………………813
Плавление Na 2 CO 3 ……………………………………………………….855
Таким образом, появление расплава (эвтектика) в шихте при температуре ниже температуры плавления соды.
Общая схема термического разложения сульфата натрия происходит по реакции:
Na 2 SO 4 (расплав)> Na 2 O (расплав) + SO 2 (газ) + 1/2 (O 2).
Окончательное разложение при температуре выше 1400 °С.
Однако, несмотря на относительно низкую температуру плавления сульфата натрия (884 °С), реакция с компонентами шихты при данной температуре затруднена. Поэтому введена предварительная стадия «раскисления» сульфата натрия путем взаимодействия его с восстановителем. И тогда первые процессы, происходящие в шихте с сернокислым натрием, представлены следующим образом:
…………………………………………………………………………………………Температура, °С
Na 2 SO 4 + 2C = Na 4 S + 2CO 3 ……………………………………..………..740-800
Na 2 S + CaCO 3 = CaS + Na 2 CO 3 …………………………………………...740-800
Образование эвтектики:
Na 2 S – Na 2 SO 4 …………………….……………………………………....740
Na 2 S – NaCO 3 ………………………………………………….………….756
NaCO 3 – CaNa 2 (CO 3) 2 ……………………………………………………780
Na 2 SO 4 – CaCO 3 …………………………………………………………..795
Na 2 SO 4 – Na 2 SiO 3 ………………………………………………..………..865
Na 2 SO 4 + CaS + 2SiO 2 = Na 2 SiO 3 + CaSiO 3 + SO 2 + S……………….865
Na 2 SO 4 + Na 2 S + 2SiO 2 = 2Na 2 SiO 3 + SO 2 + S…………………………865
Эвтектика в сульфатной шихте появляется при той же температуре, что и в содовой. Однако, когда появляется N 2 S , то в смеси Na 2 SO 4 + Na 2 S + SiO 2 он играет роль плавня, реакция начинается при 500 °С и снижается начало реакции Na 2 SO 4 + SiO 2 до 650-700 °С.
При использовании сульфатов в качестве осветлителей в стекломассе проходят сложные окислительно-восстановительные процессы, связанные с присутствием в ней нескольких элементов переменной валентности, таких как C, S, Fe. Качество осветления зависит от правильного выбранного количества вводимого в шихту осветлителя и окислительно-восстановительного состояния (ОВС) стекломассы и шихты.
Применение сульфата натрия в производстве бетона.

Сульфат натрия используется как добавка в бетон для ускорения твердения в начальные сроки.
Оптимальное содержание добавки сернокислого натрия в бетонной смеси находится в пределах 1–2% от массы цемента.
Сульфат натрия вводится в бетонную смесь, как правило, в виде водного раствора 10% концентрации, плотностью 1,092 г/см 3 . Следовательно, для введения в бетон 3,1 кг соли в виде 10% раствора на 1 м 3 смеси его потребуется: 3,1/0,1092=28,4 л. В данном количестве водного раствора соли воды содержится: 1,092х28,4-3,1=27,9 л. Таким образом, количество воды затворения с учетом водного раствора добавки для приготовления 1 м 3 бетонной смеси составит: 155-27,9=127,1 л. Аналогичные расчеты производятся и при введении добавки в количествах 1,5 и 2,0% от массы цемента.
Применение сульфата натрия для аккумулирования тепловой энергии.

Безводный сульфат натрия для этих целей не используется. Для этого используется десятиводный сульфат натрия (Na 2 SO 4 ·10H 2 O), который называется глауберовая соль или мирабилит. Источником мирабилита могут быть минералы природного происхождения или реакция безводного сульфата натрия с водой.
Данный способ теплового аккумулирования основан на фазовых переходах различных материалов. По аналогии с системой "лед-вода", в которой переход из одного состояния в другое осуществляется при 0 °С с соответствующим выделением (поглощением) тепла, плавление мирабилита в собственной кристаллизационной воде происходит при 32,4 °С с поглощением тепла при соответствующей температуре в дневное время и последующим его выделением при кристаллизации в ночные часы. Это создает возможность поддержания в теплицах температурного режима, оптимального для выращивания растений, предохраняя их от перегрева в дневные часы и от заморозков ночью.
Для снижения (повышения) температуры воздуха на 10° в теплице 3х6х3 м с учетом аккумулирования тепла в грунте и материалом теплицы, необходимо около 25 кг мирабилита.
Размещение соли в теплице в нескольких специальных относительно несложных контейнерах может обеспечить снижение температурных перегрузок в ночное время и в период максимальной солнечной
активности. Применение системы с водяным теплообменником может значительно повысить эффективность этого метода аккумулирования тепла (холода) не только в необогреваемой частной, но и в промышленной обогреваемой, теплице.
Однако, данный способ аккумулирования тепловой энергии имеет свои особенности и недостатки. Изучение которых полностью еще не окончено.
Одним из существенных недостатков мирабилита, кроме склонности к переохлаждению, является инконгруэнтный характер плавления, в результате которого происходит расслаивание твердой и жидкой фаз с выпадением в осадок гептагидрата сульфата натрия. Вследствие этого уменьшается энтальпия фазового перехода с ростом числа циклов "плавление-кристаллизация" и снижается эффективность теплообмена, связанная с осаждением твердой фазы на теплопередающую поверхность. Стабилизировать обратимость фазового перехода можно введением гетерогенных добавок в сернокислый натрий, выполняющих роль центров кристаллизации.
Цена на сульфат натрия благоприятствуют использованию его в теплоаккумулирующих составах.
Применение натрия сульфата для сушки семян.
Натрия сульфат применяют для химической сушки семян бобовых перед закладкой семян на хранение. Перед обработкой семян определяют их влажность. Для снижения влажности на каждый процент влажности берут 1,3-1,5% (по массе) натрия сульфата. Высушенные семена можно хранить до весны без отделения сульфата натрия. Всхожесть семян от этого не снижается.
Получение.
Промышленный способ получения сульфата натрия - взаимодействие NaCl с H 2 SO 4 в специальных «сульфатных» печах при 500-550 °C.
Свойства кристаллов, форма и сингония (кристаллографические системы)
Важным свойством кристалла является определенное соответствие между разными гранями - симметрия кристалла. Выделяются следующие элементы симметрии:
1. Плоскости симметрии: разделяют кристалл на две симметричные половины, такие плоскости также называют "зеркалами" симметрии.
2. Оси симметрии: прямые линии, проходящие через центр кристалла. Вращение кристалла вокруг этой оси повторяет форму исходного положения кристалла. Различают оси симметрии 3-го, 4-го и 6-го порядка, что соответствует числу таких позиций при вращении кристалла на 360 o .
3. Центр симметрии: грани кристалла, соответствующие параллельной грани, меняются местами при вращении на 180 o вокруг этого центра. Комбинация этих элементов симметрии и порядков дает 32 класса симметрии для всех кристаллов. Эти классы, в соответствии с их общими свойствами, можно объединить в семь сингонии (кристаллографических систем). По трехмерным осям координат можно определить и оценить позиции граней кристаллов.
Каждый минерал принадлежит к одному классу симметрии, поскольку имеет один тип кристаллической решетки, который его и характеризует. Напротив, минералы, имеющие одинаковый химический состав, могут образовывать кристаллы двух и более классов симметрии. Такое явление называется полиморфизмом. Есть не единичные примеры полиморфизма: алмаз и графит, кальцит и арагонит, пирит и марказит, кварц, тридимит и кристобалит; рутил, анатаз (он же октаэдрит) и брукит.
СИНГОНИИ (КРИСТАЛЛОГРАФИЧЕСКИЕ СИСТЕМЫ) . Все формы кристаллов образуют 7 сингонии (кубическую, тетрагональную, гексагональную, тригональную, ромбическую, моноклинную, триклинную). Диагностическими признаками сингонии являются кристаллографические оси и углы, образуемые этими осями.

В триклинной сингонии присутствует минимальное число элементов симметрии. За ней в порядке усложнения следуют моноклинная, ромбическая, тетрагональная, тригональная, гексагональная и кубическая сингонии.
Кубическая сингония . Все три оси имеют равную длину и расположены перпендикулярно друг другу. Типичные формы кристаллов: куб, октаэдр, ромбододекаэдр, пентагондодекаэдр, тетрагон-триоктаэдр, гексаоктаэдр.
Тетрагональная сингония . Три оси расположены перпендикулярно друг другу, две оси имеют одинаковую длину, третья (главная ось) либо короче, либо длиннее. Типичные формы кристаллов - призмы, пирамиды, тетрагоны, трапецоэдры и бипирамиды.
Гексагональная сингония . Третья и четвертая оси расположены наклонно к плоскости, имеют равную длину и пересекаются под углом 120 o . Четвертая ось, отличающаяся от остальных по размеру, расположена перпендикулярно к другим. И оси и углы по расположению аналогичны предыдущей сингонии, но элементы симметрии весьма разнообразны. Типичные формы кристаллов - трехгранные призмы, пирамиды, ромбоэдры и скаленоэдры.
Ромбическая сингония . Характерны три оси, перпендикулярные друг другу. Типичные кристаллические формы - базальные пинакоиды, ромбические призмы, ромбические пирамиды и бипирамиды.
Моноклинная сингония . Три оси разной длины, вторая перпендикулярна другим, третья находится под острым углом к первой. Типичные формы кристаллов - пинакоиды, призмы с кососрезанными гранями.
Триклинная сингония . Все три оси имеют разную длину и пересекаются под острыми углами. Типичные формы - моноэдры и пинакоиды.
Форма и рост кристаллов . Кристаллы, принадлежащие к одному минеральному виду, имеют схожий внешний вид. Кристалл поэтому можно охарактеризовать как сочетание внешних параметров (граней, углов, осей). Но относительный размер этих параметров довольно разный. Следовательно, кристалл может менять свой облик (чтобы не сказать внешность) в зависимости от степени развития тех или иных форм. Например, пирамидальный облик, где все грани сходятся, столбчатый (в совершенной призме), таблитчатый, листоватый или глобулярный.
Два кристалла, имеющих то же сочетание внешних параметров, могут иметь разный вид. Сочетание это зависит от химического состава среды кристаллизации и других условий формирования, к которым относятся температура, давление, скорость кристаллизации вещества и т. д. В природе изредка встречаются правильные кристаллы, которые формировались в благоприятных условиях - это, например, гипс в глинистой среде или минералы на стенках жеоды. Грани таких кристаллов хорошо развиты. Наоборот, кристаллы, образовавшиеся в изменчивых или неблагоприятных условиях, часто бывают деформированы.
АГРЕГАТЫ . Часто встречаются кристаллы, которым не хватало пространства для роста. Эти кристаллы срастались с другими, образуя неправильные массы и агрегаты. В свободном пространстве среди горных пород кристаллы развивались совместно, образуя друзы, а в пустотах - жеоды. По своему строению такие агрегаты весьма разнообразны. В мелких трещинах известняков встречаются образования, напоминающие окаменевший папоротник. Их называют дендритами, сформировавшимися в результате образования оксидов и гидрооксидов марганца и железа под воздействием растворов, циркулировавших в этих трещинах. Следовательно, дендриты никогда не образуются одновременно с органическими остатками.
Двойники . При формировании кристаллов часто образуются двойники, когда два кристалла одного минерального вида срастаются друг с другом по определенным правилам. Двойники часто представляют собой индивидов, сросшихся под углом. Нередко проявляется псевдосимметрия - несколько кристаллов, относящихся к низшему классу симметрии, срастаются, образуя индивиды с псевдосимметрией более высокого порядка. Так, арагонит, относящийся к ромбической сингонии, часто образует двойниковые призмы с гексагональной псевдосимметрией. На поверхности таких срастаний наблюдается тонкая штриховка, образованная линиями двойникования.
ПОВЕРХНОСТЬ КРИСТАЛЛОВ . Как уже сказано, плоские поверхности редко бывают гладкими. Довольно часто на них наблюдается штриховка, полосчатость или бороздчатость. Эти характерные признаки помогают при определении многих минералов - пирита, кварца, гипса, турмалина.
ПСЕВДОМОРФОЗЫ . Псевдоморфозы - это кристаллы, имеющие форму другого кристалла. Например, встречается лимонит в форме кристаллов пирита. Псевдоморфозы образуются при полном химическом замещении одного минерала другим с сохранением формы предыдущего.


Формы
агрегатов
кристаллов
могут быть
очень
разнообразны.
На фото -
лучистый
агрегат
натролита.
Образец
гипса
со сдвойникованными
кристаллами
в виде креста.
Физические и химические свойства. Не только внешняя форма и симметрия кристалла определяются законами кристаллографии и расположением атомов - это относится и к физическим свойствам минерала, которые могут быть разными в различных направлениях. Например, слюда может разделяться на параллельные пластинки только в одном направлении, поэтому ее кристаллы анизотропны. Аморфные вещества одинаковы по всем направлениям, и поэтому изотропны. Такие качества также важны для диагностики этих минералов.
Плотность. Плотность (удельный вес) минералов представляет собой отношение их веса к весу такого же объема воды. Определение удельного веса является важным средством диагностики. Преобладают минералы с плотностью 2-4. Упрощенная оценка веса поможет при практической диагностике: легкие минералы имеют вес от 1 до 2, минералы средней плотности - от 2 до 4, тяжелые минералы от 4 до 6, очень тяжелые - более 6.
МЕХАНИЧЕСКИЕ СВОЙСТВА . К ним относятся твердость, спайность, поверхность скола, вязкость. Эти свойства зависят от кристаллической структуры и используются с целью выбора методики диагностирования.
ТВЕРДОСТЬ . Довольно легко поцарапать кристалл кальцита кончиком ножа, но сделать это с кристаллом кварца вряд ли получится - лезвие скользнет по камню, не оставив царапины. Значит, твердость у этих двух минералов различная.
Твердостью по отношению к царапанью называют сопротивление кристалла попытке внешней деформации поверхности, другими словами, сопротивление механической деформации извне. Фридрих Моос (1773-1839) предложил относительную шкалу твердости из степеней, где каждый минерал имеет твердость к процарапыванию выше, чем предыдущий: 1. Тальк. 2. Гипс. 3. Кальцит. 4. Флюорит. 5. Апатит. 6. Полевой шпат. 7. Кварц. 8. Топаз. 9. Корунд. 10. Алмаз. Все эти значения применимы только к свежим, не подвергшимся выветриванию образцам.
Можно оценить твердость упрощенным способом. Минералы с твердостью 1 легко царапаются ногтем; при этом они жирные на ощупь. Поверхность минералов с твердостью 2 также царапается ногтем. Медная проволока или кусочек меди царапает минералы с твердостью 3. Кончик перочинного ножа царапает минералы до твердости 5; хороший новый напильник - кварц. Минералы с твердостью более 6 царапают стекло (твердость 5). От 6 до 8 не берет даже хороший напильник; при таких попытках летят искры. Чтобы определить твердость, испытывают образцы с возрастающей твердостью, пока они поддаются; затем берут образец, который, очевидно, еще тверже. Противоположным образом надо действовать, если необходимо определить твердость минерала, окруженного породой, твердость которой ниже, чем у минерала, нужного для образца.


Тальк и алмаз, два минерала, занимающие крайние позиции в шкале твердости Мооса.
Легко сделать вывод на основании того, скользит ли минерал по поверхности другого или царапает ее с легким скрипом. Могут наблюдаться следующие случаи:
1. Твердость одинакова, если образец и минерал взаимно не царапают друг друга.
2. Возможно, что оба минерала
друг друга царапают, поскольку
верхушки и выступы кристалла
могут быть тверже, чем грани или
плоскости спайности. Поэтому
можно поцарапать грань кристалла гипса или плоскость его спайности вершиной другого кристалла гипса.
3. Минерал царапает первый образец, а на нем делает царапину
образец более высокого класса твердости. Его твердость находится посредине между используемыми для сравнения образцами, и ее можно оценить в полкласса.
Несмотря на очевидную простоту такого определения твердости, многие факторы могут привести к ложному результату. Например, возьмем минерал, свойства которого сильно разнятся по разным направлениям, как у дистена (кианита): по вертикали твердость 4-4,5, и кончик ножа оставляет четкий след, но в перпендикулярном направлении твердость 6-7 и ножом минерал вообще не царапается. Происхождение названия этого минерала связано с этой особенностью и подчеркивает ее весьма выразительно. Поэтому необходимо проводить испытание твердости по разным направлениям.
Некоторые агрегаты имеют более высокую твердость, чем те компоненты (кристаллы или зерна), из которых они состоят; может оказаться, что плотный обломок гипса трудно поцарапать ногтем. Наоборот, некоторые пористые агрегаты менее твердые, что объясняется наличием пустот между гранулами. Поэтому мел царапается ногтем, хотя состоит из кристаллов кальцита с твердостью 3. Другой источник ошибок - минералы, испытавшие какие-то изменения. Оценить твердость порошкообразных, выветрелых образцов или агрегатов чешуйчатого и игольчатого строения простыми средствами невозможно. В таких случаях лучше использовать другие методы.
 Спайность
. Ударом молотка или нажатием ножа кристаллы по плоскостям спайности кристалл иногда можно разделить на пластинки. Спайность проявляется по плоскостям с минимальным сцеплением. Многие минералы обладают спайностью по нескольким направлениям: галит и галенит - параллельно граням куба; флюорит - по граням октаэдра, кальцит - ромбоэдра. Кристалл слюды-мусковита; хорошо видны плоскости спайности (на фото справа).
Спайность
. Ударом молотка или нажатием ножа кристаллы по плоскостям спайности кристалл иногда можно разделить на пластинки. Спайность проявляется по плоскостям с минимальным сцеплением. Многие минералы обладают спайностью по нескольким направлениям: галит и галенит - параллельно граням куба; флюорит - по граням октаэдра, кальцит - ромбоэдра. Кристалл слюды-мусковита; хорошо видны плоскости спайности (на фото справа).
Такие минералы, как слюда и гипс, имеют совершенную спайность в одном направлении, а в других направлениях спайность несовершенная или вообще отсутствует. При тщательном наблюдении можно заметить внутри прозрачных кристаллов тончайшие плоскости спайности по хорошо выраженным кристаллографическим направлениям.
Поверхность излома . Многие минералы, например кварц и опал, не имеют спайности ни в одном направлении. Их основная масса раскалывается на неправильные куски. Поверхность скола можно описать как плоскую, неровную, раковистую, полураковистую, шероховатую. Металлы и крепкие минералы имеют шероховатую поверхность скола. Это свойство может служить диагностическим признаком.
Другие механические свойства . Некоторые минералы (пирит, кварц, опал) раскалываются на куски под ударом молотка - они являются хрупкими. Другие, наоборот, превращаются в порошок, не давая обломков.
Ковкие минералы можно расплющить, как, например, чистые самородные металлы. Они не образуют ни порошка, ни обломков. Тонкие пластинки слюды можно согнуть, как фанеру. После прекращения воздействия они вернутся в исходное состояние - это свойство эластичности. Другие, как гипс и пирит, можно согнуть, но они сохранят деформированное состояние - это свойство гибкости. Такие признаки позволяют распознавать сходные минералы - например, отличить эластичную слюду от гибкого хлорита.
Окраска . Некоторые минералы имеют настолько чистый и красивый цвет, что их используют как краски или лаки. Часто их названия применяют в обиходной речи: изумрудно-зеленый, рубиново-красный, бирюзовый, аметистовый и др. Окраска минералов, один из основных диагностических признаков, не является ни постоянной, ни вечной.
Есть ряд минералов, у которых окраска постоянная - малахит всегда зеленый, графит - черный, самородная сера - желтая. Такие распространенные минералы, как кварц (горный хрусталь), кальцит, галит (поваренная соль), бесцветны, когда в них нет примесей. Однако наличие последних вызывает окраску, и мы знаем голубую соль, желтый, розовый, фиолетовый и коричневый кварц. Флюорит обладает целой гаммой окрасок.
 Присутствие элементов-примесей в химической формуле минерала приводит к весьма специфической окраске. На этой фотографии изображен зеленый кварц (празем), в чистом виде совершенно бесцветный и прозрачный.
Присутствие элементов-примесей в химической формуле минерала приводит к весьма специфической окраске. На этой фотографии изображен зеленый кварц (празем), в чистом виде совершенно бесцветный и прозрачный.
Турмалин, апатит и берилл имеют различные цвета. Окраска не является несомненным диагностическим признаком минералов, обладающих различными оттенками. Цвет минерала зависит также от наличия элементов-примесей, входящих в кристаллическую решетку, а также различных пигментов, загрязнений, включений в кристалле-хозяине. Иногда он может быть связан с радиоактивным облучением. У некоторых минералов цвет меняется в зависимости от освещения. Так, александрит при дневном свете зеленый, а при искусственном освещении - фиолетовый.
У некоторых минералов изменяется интенсивность окраски при повороте граней кристалла относительно света. Цвет кристалла кордиерита при вращении меняется от голубого до желтого. Причина такого явления состоит в том, что подобные кристаллы, называемые плеохроичными, по-разному поглощают свет в зависимости от направления луча.
Цвет некоторых минералов может изменяться также при наличии пленки, имеющей другую окраску. Эти минералы в результате окисления покрываются налетом, который, возможно, как-то смягчает действие солнечного или искусственного света. Некоторые драгоценные камни теряют свою окраску, если в течение какого-то периода подвергаются солнечному освещению: изумруд теряет свой глубокий зеленый цвет, аметист и розовый кварц бледнеют.
Многие минералы, содержащие серебро (например, пираргирит и прустит), также чувствительны к солнечным лучам (инсоляции). Апатит под воздействием инсоляции покрывается черной вуалью. Коллекционерам следует предохранять такие минералы от воздействия света. Красный цвет реальгара на солнце переходит в золотисто-желтый. Подобные изменения окраски совершаются в природе очень медленно, но можно искусственно очень быстро изменить цвет минерала, ускорив процессы, происходящие в природе. Например, можно при нагревании получить желтый цитрин из фиолетового аметиста; алмазы, рубины и сапфиры искусственно "улучшают" с помощью радиоактивного облучения и ультрафиолетовых лучей. Горный хрусталь благодаря сильному облучению превращается в дымчатый кварц. Агат, если его серый цвет выглядит не слишком привлекательно, можно перекрасить, опустив в кипящий раствор обыкновенного анилинового красителя для тканей.
ЦВЕТ ПОРОШКА (ЧЕРТА) . Цвет черты определяется при трении о шероховатую поверхность неглазированного фарфора. При этом нужно не забывать, что фарфор имеет твердость 6-6,5 по шкале Мооса, и минералы с большей твердостью оставят только белый порошок растертого фарфора. Всегда можно получить порошок в ступке. Окрашенные минералы всегда дают более светлую черту, неокрашенные и белые - белую. Обычно белая или серая черта наблюдается у минералов, окрашенных искусственно, или с загрязнениями и пигментом. Часто она как бы затуманена, так как в разбавленной окраске ее интенсивность обуславливается концентрацией красящего вещества. Цвет черты минералов с металлическим блеском отличается от их собственного цвета. Желтый пирит дает зеленовато-черную черту; черный гематит - вишнево-красную, черный вольфрамит - коричневую, а касситерит - почти неокрашенную черту. Цветная черта позволяет быстрее и легче определить по ней минерал, чем черта разбавленного цвета или бесцветная.
БЛЕСК . Как и цвет, это эффективный метод определения минерала. Блеск зависит оттого, как свет отражается и преломляется на поверхности кристалла. Различают минералы с металлическим и неметаллическим блеском. Если их различить не удается, можно говорить о полуметаллическом блеске. Непрозрачные минералы металлов (пирит, галенит) обладают большой отражательной способностью и имеют металлический блеск. Для другой важной группы минералов (цинковая обманка, касситерит, рутил и др.) определить блеск затруднительно. Для минералов с неметаллическим блеском различают следующие категории в соответствии с интенсивностью и свойствами блеска:
1. Алмазный блеск, как у алмаза.
2. Стеклянный блеск.
3. Жирный блеск.
4. Тусклый блеск (у минералов с плохой отражательной способностью).
Блеск может быть связан со строением агрегата и направлением господствующей спайности. Минералы, имеющие тонкослоистое сложение, имеют перламутровый блеск.
ПРОЗРАЧНОСТЬ . Прозрачность минерала - качество, которое отличается большой изменчивостью: непрозрачный минерал можно легко отнести к прозрачным. Основная часть бесцветных кристаллов (горный хрусталь, галит, топаз) относятся к этой группе. Прозрачность зависит от строения минерала - некоторые агрегаты и мелкие зерна гипса и слюды кажутся непрозрачными или просвечивающими, в то время как кристаллы этих минералов прозрачны. Но если рассматривать с лупой маленькие гранулы и агрегаты, можно видеть, что они прозрачны.
ПОКАЗАТЕЛЬ ПРЕЛОМЛЕНИЯ . Показатель преломления представляет собой важную оптическую константу минерала. Она измеряется с помощью специальной аппаратуры. Когда луч света проникает внутрь анизотропного кристалла, происходит преломление луча. Такое двойное лучепреломление создает впечатление, что существует виртуальный второй объект параллельно изучаемому кристаллу. Подобное явление можно наблюдать через прозрачный кристалл кальцита.
ЛЮМИНЕСЦЕНЦИЯ . Некоторые минералы, такие как шеелит и виллемит, облучаемые ультрафиолетовыми лучами, светятся специфическим светом, что в ряде случаев может некоторое время продолжаться. Флюорит при нагревании в темном месте светится - это явление называется термолюминесценция. При трении некоторых минералов возникает другой тип свечения - триболюминесценция. Эти разные типы люминесценции являются характеристикой, позволяющей легко диагностировать ряд минералов.
ТЕПЛОПРОВОДНОСТЬ . Если взять в руку кусок янтаря и кусок меди, покажется, что один из них теплее другого. Это впечатление обусловлено различной теплопроводностью данных минералов. Так можно различить стеклянные имитации драгоценных камней; для этого нужно приложить камушек к щеке, где кожа более чувствительна к теплу.
Следующие свойства можно определить по тому, какие ощущения они вызывают у человека. На ощупь графит и тальк кажутся гладкими, а гипс и каолин - сухими и шероховатыми. Растворимые в воде минералы, такие как галит, сильвинит, эпсомит, имеют специфический вкус - соленый, горький, кислый. Некоторые минералы (сера, арсенопирит и флюорит) обладают легко распознаваемым запахом, который возникает сразу при ударе по образцу.
МАГНЕТИЗМ . Фрагменты или порошок некоторых минералов, в основном имеющих повышенное содержание железа, можно отличить от других сходных минералов с помощью магнита. Магнетит и пирротин сильно магнитны и притягивают железные опилки. Некоторые минералы, например гематит, приобретают магнитные свойства, если их раскалить докрасна.
ХИМИЧЕСКИЕ СВОЙСТВА . Определение минералов на основе их химических свойств требует, помимо специального оборудования, обширных знаний в области аналитической химии.
Есть один простой метод для определения карбонатов, доступный непрофессионалам - действие слабого раствора соляной кислоты (вместо нее можно брать обыкновенный столовый уксус - разбавленную уксусную кислоту, которая есть на кухне). Таким способом можно легко отличить бесцветный образец кальцита от белого гипса - нужно капнуть на образец кислоты. Гипс на это не реагирует, а кальцит "вскипает" при выделении углекислого газа.
Прижигающие свойства нитрата серебра используются в медицине для удаления мелких бородавок и прижигания мелких ранок. Нитрат серебра применяется в альтернативной медицине – гомеопатии, как действующее вещество.Нитрат серебра это вещество, которое было известно еще в средневековье. Оно имело, широкое распространение и было особенно популярно среди медиков, химиков и алхимиков. Нитрат серебра проник во все языковые культуры цивилизованных стран Азии и Европы. Упоминание о нем есть не только в научной, но в медицинской и художественной литературе. В средние века ляпис часто называли "адским камнем". Такое название ляпис, очевидно, получил из-за своих свойств - прижигать ткани. При прижигании кожи, ляпис вызывает коагуляцию белка и некроз (омертвление) кожной ткани. В беллетристике средневековья, ляпис чаще упоминался как "адский камень" и реже как ляпис.
Основные свойства нитрата серебра (AgNO3)
Ляпис может вызвать бытовое отравление
Клинические проявления характерные при отравлении ляписом: ожог слизистой оболочки полости рта, пищевода, желудка, понос, падение артериального давления, головокружение, судороги, кашель с обильным выделением мокроты, тошнота, рвота белыми массами и темнеющими на свету, нарушение дыхания, анурия и кома.Сульфат калия является неорганическим соединением с химической формулой K2SO4.
Как пищевая добавка сульфат калия имеет название Е515 и относится к группе эмульгаторов, которые необходимы для создания однородной смеси из несмешиваемых в природе компонентов, например, воды с маслом или воды с жиром. Также Е515 применяется при промышленном производстве продуктов для регулирования кислотности.
Сульфат калия является жесткой и горькой солью с очень высокой температурой плавления (около 1078°C). Он представляет собой бесцветные ромбические кристаллы, легко растворимые в воде.
Получение сульфата калия
Сульфат калия как химическое соединение был известен с начала 14 века благодаря химикам Бойлу, Глауберу и Тахеусу.
В природе сульфат калия встречается на месторождениях калийных солей. Кроме того, он присутствует в водах соленых озер, однако, в большинстве случаев, с различными примесями. Чистый сульфат калия находится в природе относительно редко. Самым известным его природным источником является минерал арканит в виде белых или прозрачных кристаллов, который встречается в Калифорнии (США).
Получение сульфата калия возможно из природных минералов, его содержащих. К ним относятся шенит, каинит, леонит, сингенит, глазерит, лангбейнит и полигалит.
В лабораторной практике для получения сульфата калия используют реакции с оксидом калия, со слабыми или неустойчивыми кислотами и некоторые другие.
Свойства сульфата калия
Сульфат калия является необходимым соединением для организма, поскольку он участвует в процессе доставки кислорода к клеткам.
Нехватка сульфата калия отражается не только на состоянии кожи и волос, но и на общем тонусе организма, что проявляется как быстрая утомляемость.
В продуктах сульфат калия содержится в морской капусте, шпинате, сыре, свекле, нежирной говядине, бананах, цитрусовых (лимонах и апельсинах), миндале.
Сульфат калия как химическое соединение небезопасен для организма в случаях:
- При попадании в глаза и на кожу – возможно механическое раздражение;
- При проглатывании большого количества сульфата калия – возможно раздражение желудочно-кишечного тракта;
- При вдыхании соединения – возможно раздражение дыхательных путей.
Применение сульфата калия в пищевой промышленности
 При промышленном производстве продуктов питания сульфат калия как добавка Е515 чаще всего используется как заменитель соли, а также:
При промышленном производстве продуктов питания сульфат калия как добавка Е515 чаще всего используется как заменитель соли, а также:
- Как питательная среда при приготовлении ржаных заквасок и дрожжей жидкой консистенции;
- Как регулятор кислотности в напитках;
- Как источник питания минералами.
Сульфат калия в умеренных количествах полезен для организма. Однако чрезмерное его количество может привести к расстройству желудка, раздражению всего пищеварительного тракта, а в некоторых случаях – к отравлению организма.
Применение сульфата калия
Сульфат калия широко применяют в сельском хозяйстве в виде бесхлорного удобрения. Эффективность раствора сульфата калия наиболее высока на дерново-подзолистых и торфяных почвах, которые бедны калием. Также его используют как альтернативу удобрениям с содержание хлора для выращивания табака, картофеля, винограда, льна, цитрусовых.
На черноземных почвах раствор сульфата калия применят, как правило, под культуры, усваивающие много натрия и калия, среди которых подсолнечник, сахарная свекла, плодовые, различные корнеплоды и овощи.
Наиболее эффективен раствор сульфата калия в сочетании с азотными и фосфорными удобрениями.
Также сульфат калия применяют:
- В фармакологии – в качестве сырья для производства биологически активных добавок;
- В стекольном производстве.